催化不对称N-H键插入反应合成非天然氨基酸酯
南开大学化学学院朱守非课题组发展了一种基于催化卡宾对N-H键的插入反应合成非天然氨基酸酯的新方法。该方法以Tp*Cu(I)配合物与手性磷酸为催化剂,α-烷基重氮酯为卡宾前体,氨基甲酸酯为N-H键给体,高收率和高对映选择性地合成了胺基甲酸酯基保护的非天然α-氨基酸酯,具有条件温和、底物适用范围广、官能团耐受性好等特点,丰富了非天然氨基酸的类型。该方法合成的保护的非天然氨基酸具有很好的应用潜力,可对映选择性保持地转化为多种α-氨基酸衍生物,并可直接应用于人工合成多肽。该研究拓展了N-H键插入反应,丰富了非天然氨基酸类型,为非天然多肽的合成应用和功能发现提供了新的物质基础。相关成果近期发表于ACS Catal. (2022, 12, DOI: 10.1021/acscatal.2c03937),博士生李游、本科生苏楀轩是文章共同第一作者。

多肽是一类具有重要生物活性的物质,可用于制作疫苗和药物,其中非天然多肽通常表现出不同于天然多肽的生物活性,因而其合成广受关注。用固相合成法制备非天然多肽时,一般要用到N,C端双保护的非天然氨基酸,其中N端保护基最常见的是胺基甲酸酯。α-重氮酯衍生的卡宾和胺基甲酸酯的不对称N-H键插入反应是合成氨基甲酸酯保护的非天然α-氨基酸酯的直接方法,此前人们实现了α-芳基和α-烯基重氮酯衍生卡宾对胺基甲酸酯N-H键的高对映选择性插入反应,但α-烷基重氮酯衍生卡宾的同类反应仍然没有成功的例子。这可能是由于在金属催化下,α-烷基卡宾容易发生β-H迁移反应得到烯烃副产物,而其烷基相较芳基和烯基柔性更高,造成相应N-H键插入反应的对映选择性控制更为困难。
朱守非课题组发展了一系列手性质子梭催化剂促进的卡宾不对称插入反应(J. Am. Chem. Soc. 2020, 142, 10557; Science 2019, 366, 990; Acta Chim. Sinica. 2018, 76, 883; Chem. Sci. 2016, 7, 1104; J. Am. Chem. Soc. 2015, 137, 8700; Angew. Chem. Int. Ed. 2014, 53, 3913; Chem. Sci. 2014, 5, 1442; Angew. Chem. Int. Ed. 2011, 50, 11483),作为这一方向的最新进展,近期他们使用α-烷基重氮酯作为卡宾前体,在温和条件下,实现了Tp*Cu(I)配合物与手性磷酸催化对胺基甲酸酯N-H键的不对称插入反应,高收率及高对映选择性地合成了系列氨基甲酸酯保护的非天然α-氨基酸酯。该合成方法具有操作简单、反应条件温和、底物范围广、官能团耐受性好等特点。该反应方法学拓展了催化卡宾对N-H键的不对称插入反应,丰富了非天然氨基酸的种类,为其在非天然多肽合成中的应用提供了新的物质基础。
该反应具有广泛的底物适用范围,氨基甲酸甲酯、叔丁酯(Boc保护基)、环戊酯、苄酯(Cbz保护基)、以及9-芴基甲酯(Fmoc保护基)都适用;烷基端含有支链、炔烃、烯烃、苯基、硅基、环丙基时也都能给出很好的结果(图1)。
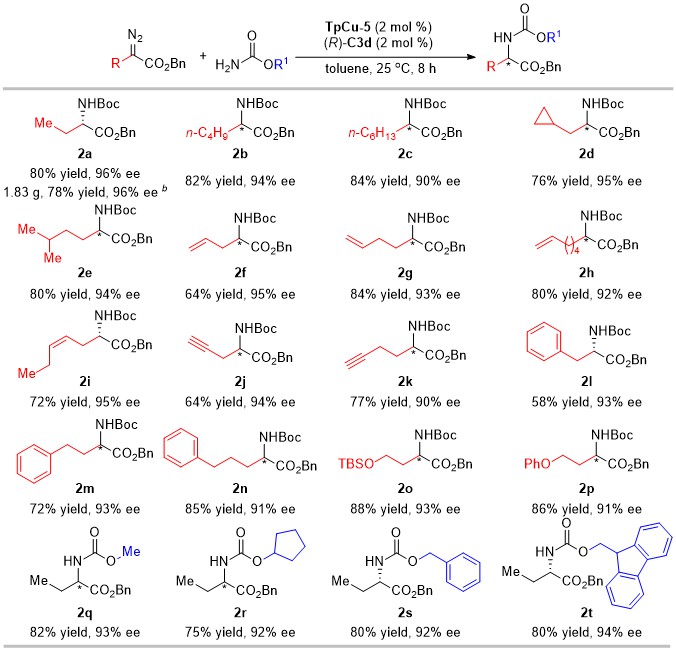
图1 底物适用范围
该反应具有较好的应用潜力。反应可以放大到克级规模,收率和对映选择性都能很好的保持。所得保护的氨基酸能进行多种对映选择性保持的转化,还可作为天然产物及生物活性分子的重要合成子(图2)。
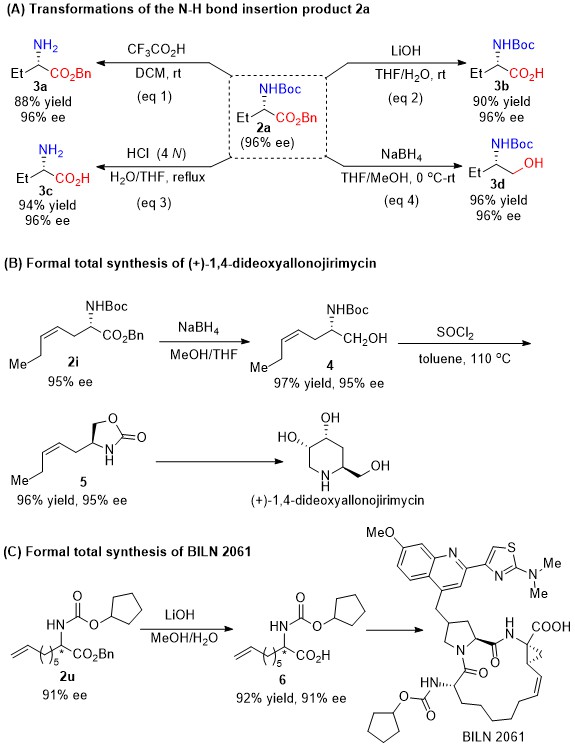
图2 合成应用展示
参考其它O-H或N-H键插入反应的机理,研究者提出了可能的催化路径(图3)。首先,α-烷基重氮酯在铜催化剂作用下分解重氮得到铜卡宾CB,随后发生分步的N-H键插入过程,经历两个过渡态NHi-TS-1和NHi-TS-2,得到烯醇中间体,最后手性磷酸作为质子梭催化剂,促进烯醇中间体发生协同的质子转移过程,给出插入产物胺基甲酸酯保护的α-烷基-α-氨基酸酯。
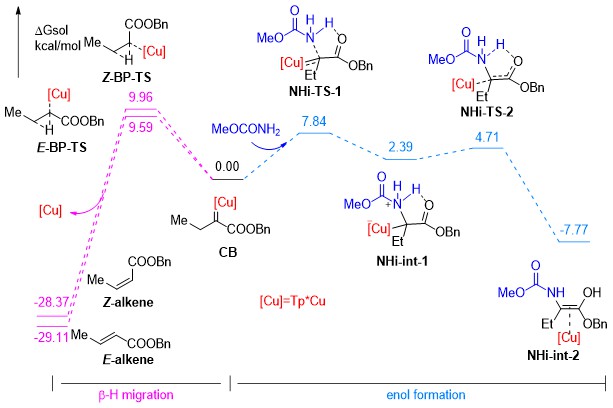
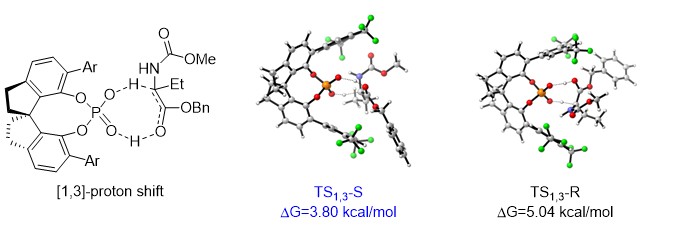
图3 建议机理
计算结果表明,本反应的选择性控制步骤主要由两步组成:第一是N-H插入过程中,催化剂配体对底物不发生插入的氢的额外氢键作用(图4中绿色区域),使得插入反应的活化能进一步降低,阻止了β-H迁移副反应的发生。第二是手性磷酸催化质子转移过程中,由于生成R构型的产物在过渡态中需要催化剂空腔更大幅度的变形(图4),造成了更明显的能量升高,导致反应产物具有S选择性。
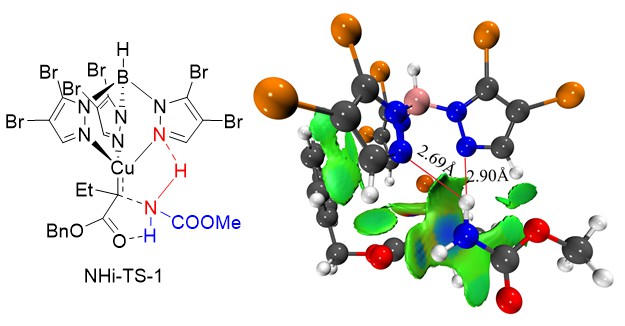
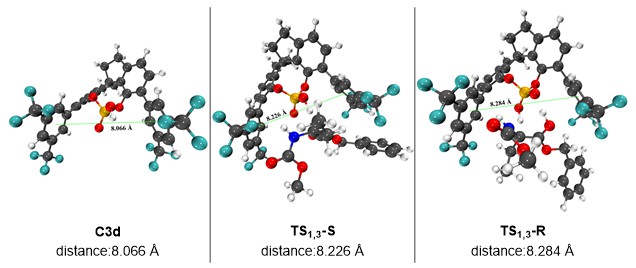
图4 计算结果与解析
总之,本研究发展了Tp*Cu配合物与手性磷酸协同催化的新体系,首次实现了α-烷基重氮酯衍生的卡宾对氨基甲酸酯的N-H键的不对称插入反应,以高收率和高对映选择性得到了氨基甲酸酯保护的非天然α-氨基酸酯。该反应条件温和,产物稳定性好,底物范围广,为非天然氨基酸的合成提供了新的实用的方法。本研究合成的非天然氨基酸酯可对映选择性保持地合成多种氨基酸衍生物,可用于生物活性分子的合成,也为非天然多肽的合成提供了新的物质基础。
