Wittig/B-H插入反应:合成Z式三取代烯烃的新策略
Wittig反应是从羰基化合物合成烯烃最有效的方法之一,该反应一般生成热力学稳定的E-烯烃。南开大学化学学院朱守非课题组报道了一例Wittig/B-H插入反应,创新性地将Wittig反应与卡宾对B-H键的插入反应结合在一起,提供了一种从酮出发合成热力学不稳定的三取代Z-烯基硼化合物的新方法,具有条件温和,原料易得,立体选择性高,官能团耐受性好等特点。结合硼基团的简易转化,该方法提供了获得以前无法合成的多种三取代Z-烯烃的高效途径,从而为药物发现提供了新的机遇。同时,该方法还可以用于分子内反应,合成具有单环、稠环、螺环结构的新型B-N杂环和B-P杂环化合物,为新型含硼功能分子的发现提供了物质基础。机理研究表明,该反应独特的Z式选择性是由硼烷加合物的B-H键与过渡态中的亚烷基卡宾中间体之间轨道的最大重叠决定的。该成果近期发表于Sci. Adv. 2023, 9, eadj2486,博士生郭风开是文章的第一作者。
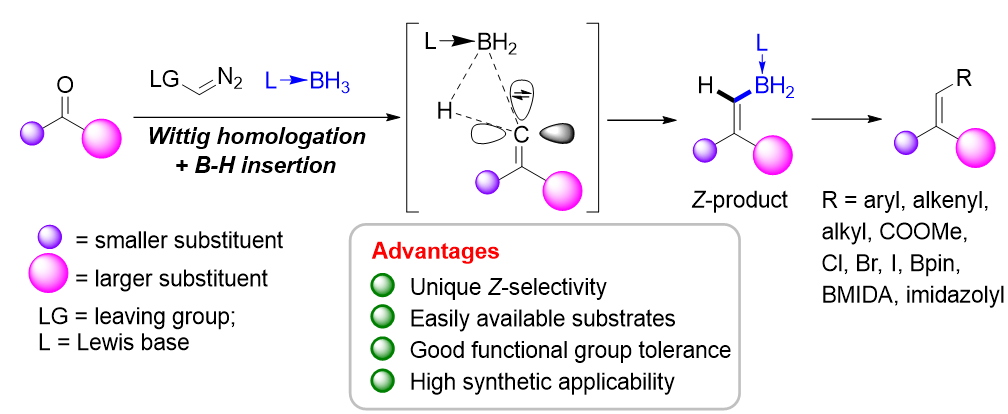
图1. Wittig/B-H插入反应
烯烃是一类重要的有机化合物,发展烯烃的合成新方法一直是化学家们关注的焦点。Wittig反应作为一类高效合成烯烃的方法,具有原料易得、底物适用范围广、官能团耐受性好、产率高、操作简单等优点,是最可靠、最实用的烯烃合成方法之一。然而,该方法通常给出热力学稳定的E式构型烯烃产物,在热力学不稳定的Z式构型的选择性合成方面仍存在一些困难,尤其在以酮为底物合成三取代Z式烯烃方面,存在巨大挑战。目前,酮的Z式选择性Wittig反应只能通过使用高活性的烷基Wittig试剂来实现,因而其产物类型局限性很大(图 2A)。因此,开发合成Z-三取代烯烃的合成新策略具有重要意义。
此前,南开大学朱守非课题组报道了一系列卡宾对B-H键的插入反应,可以高效合成多种新型有机硼化合物(J. Am. Chem. Soc., 2013, 135, 14094-14097; Acta Chim. Sinica. 2015, 73, 326-329; J. Am. Chem. Soc, 2017, 139, 3784-3789; ACS Catal. 2018, 8, 7351-7355; J. Am. Chem. Soc. 2018, 140, 10663-10668; J. Am. Chem. Soc. 2020, 142, 20924-20929; CCS Chem. 2021, 3, 1721-1726; Angew. Chem. Int. Ed. 2021, 60, 24214-24219; Angew. Chem. Int. Ed. 2022, 61, e202203343; ACS Catal. 2022, 12, 10654–10660; Chem. Sci. 2023, DOI: 10.1039/D3SC03266C)。在上述研究的基础上,他们于本工作中报道了一类新型的Wittig/B-H插入反应。通过该方法,可以在温和的反应条件下,以易于获得的二烷基酮、重氮甲基磷酸二甲酯或三甲基硅基重氮甲烷以及路易斯碱-硼烷加合物为原料,方便地合成一系列热力学不稳定的新型三取代Z-烯基硼化合物(图 2B)。通过对产物中的硼取代基进行立体特异性转化,制备出了以前无法获得的多种三取代Z式烯烃。此外,通过分子内Wittig/B-H插入反应还顺利制备出了5-8元B-N或B-P杂环化合物,其中大多数化合物无法用此前已知方法合成,为新型含硼功能分子的发现提供了物质基础。
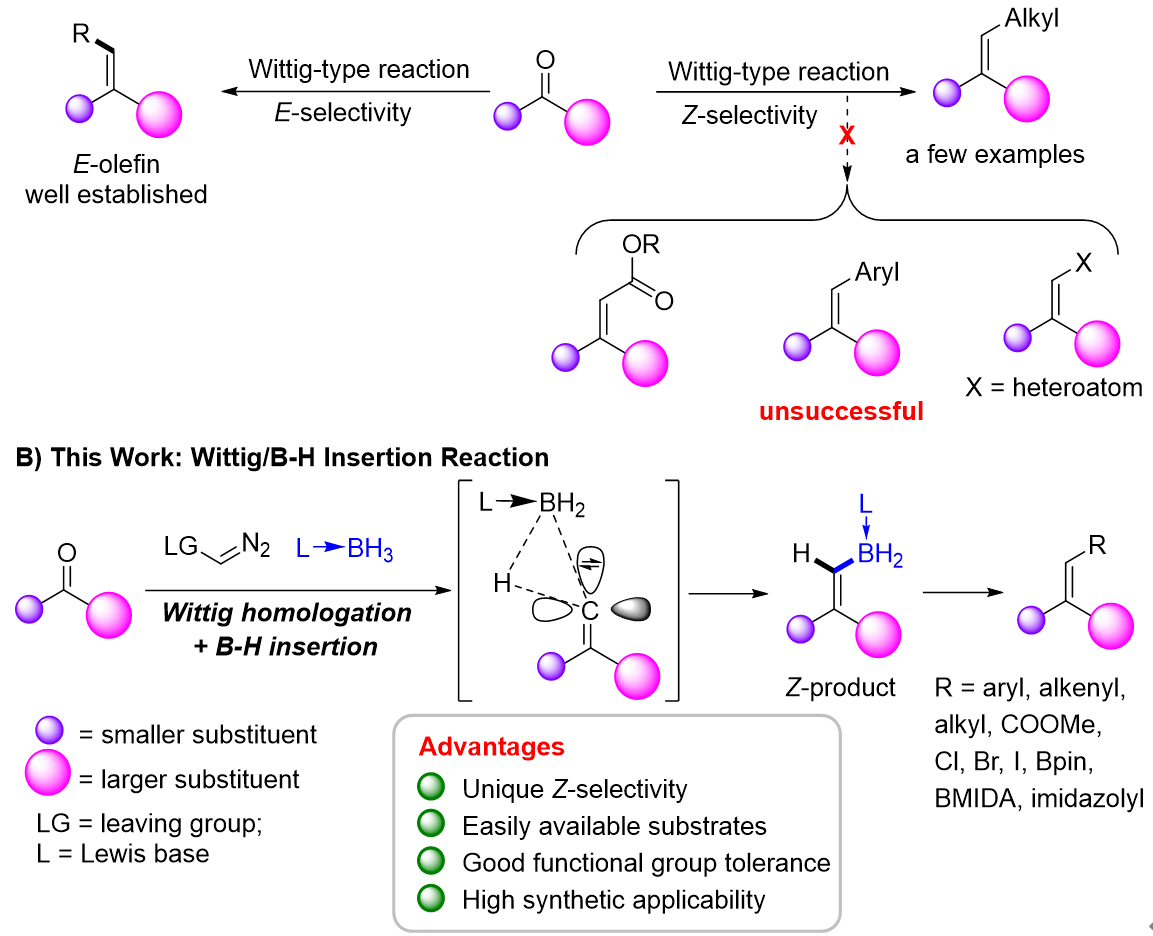
图2. Z式烯烃的合成
该反应使用双烷基酮作为底物,重氮甲基磷酸二甲酯作为Wittig试剂,叔丁醇钠作为碱,硼烷-三甲胺作为硼试剂,-78 - -40 oC下反应2小时,即可得到目标烯基硼产物(图3)。对不对称脂肪酮(R1 ≠ R2),增加R1和R2之间的立体位阻差异,即可获得优异的立体选择性。反应的底物适用范围较广,许多类固醇及其衍生物可以成功应用于该反应中,给出良好的产率和优异的Z选择性。在酮的芳基上引入具有不同电性的取代基以及稠环、芳杂环和炔基取代基对反应的产率和立体选择性没有明显影响。将反应扩大至克级规模时,产率和选择性都得到了很好的保持。
各类对称的酮,包括环酮和链状酮都适用于该反应,在标准条件下顺利给出目标的烯基硼化合物(图4A)。
分子内的Wittig/B-H插入反应也可以顺利发生(图4B),给出相应的非芳香性含硼杂环化合物。当在底物酮中引入胺-硼烷取代基时,可以得到B-N杂环戊烯或环己烯化合物,产物可以是多取代并环、螺环化合物。当在底物酮中引入膦-硼烷取代基时,可以得到5元或6元B-P杂环化合物。值得注意的是,这些化合物大部分都未见报道。

图3. 分子间Wittig/B-H插入反应底物适用范围
该反应具有优异的官能团耐受性,可以耐受醚、硫醚、烷基胺、芳基胺、磺酰胺、酰胺、硅烷基、酯基、羟基、磺酸基、羰基、硝基和腈基等官能团,这为其实际的合成应用提供了良好基础。

图4. 对称酮和分子内Wittig/B-H插入反应
产物中的C-B键可方便地进行卤代、偶联、加成等多种反应,转化为C-C键和多种官能团,转化过程中双键的构型都能很好保持,这表明本方法具有很好的合成应用潜力(图5)。值得注意的是,这里合成的大部分Z-烯烃产物都很难直接通过Wittig反应合成。

图5. 产物转化
在反应机理方面,作者通过氘代实验证明,反应的亚烷基卡宾对B-H的插入过程可能经历协同过程,并通过加入TEMPO作为自由基捕获剂排除了自由基历程(图6A)。作者提出反应经历三个阶段(图6B),首先叔丁醇钠对重氮甲基膦酸二甲酯脱氢生成碳负离子,碳负离子在Na+的作用下进攻羰基碳,经历Wittig过程脱氧得到亚烷基重氮化合物,然后脱重氮得到亚烷基卡宾中间体。硼烷加合物中富电子的氢靠近卡宾的空轨道,随后经历三元环过渡态得到B-H插入产物。反应的选择性是在卡宾对B-H键的插入过程产生的。最后,作者通过DFT计算对反应选择性的产生给出了解释(图6C)。在插入反应过程中,亚烷基卡宾以单线态形式参与反应,其孤对电子分布于卡宾碳的顶端,此时孤对电子和卡宾双键相互远离,排斥最小。在B-H键的插入过程中,硼烷加合物的富电子氢与卡宾碳原子一侧的空轨道结合,形成络合物,紧接着经过一个三元环过渡态,电子从硼氢键流向碳氢键,同时硼原子转移到碳原子上。由于Ts-1中卡宾双键的取代基对硼烷加合物的位阻效应比其他情况下都要小,因此这个过渡态中卡宾碳与硼和氢的中心轨道的重叠程度比其他任何过渡态中都要大。以此为标准,在Z和E选择性插入的过渡态中,前者的轨道重叠程度要大于后者,因此可以认为E式选择性过渡态的成键轨道重叠程度更低,成键时需要克服更高的能垒。通过IRI分析作者发现,插入过程的阻力主要存在于卡宾碳对硼烷加合物配位的Lewis碱的位阻作用及硼原子与亚烷基卡宾取代基之间的相互作用。对于两种选择性的过渡态来说,硼原子与亚烷基卡宾取代基之间的相互作用存在比较明显的差异,Z式选择性的过渡态排斥力更小。
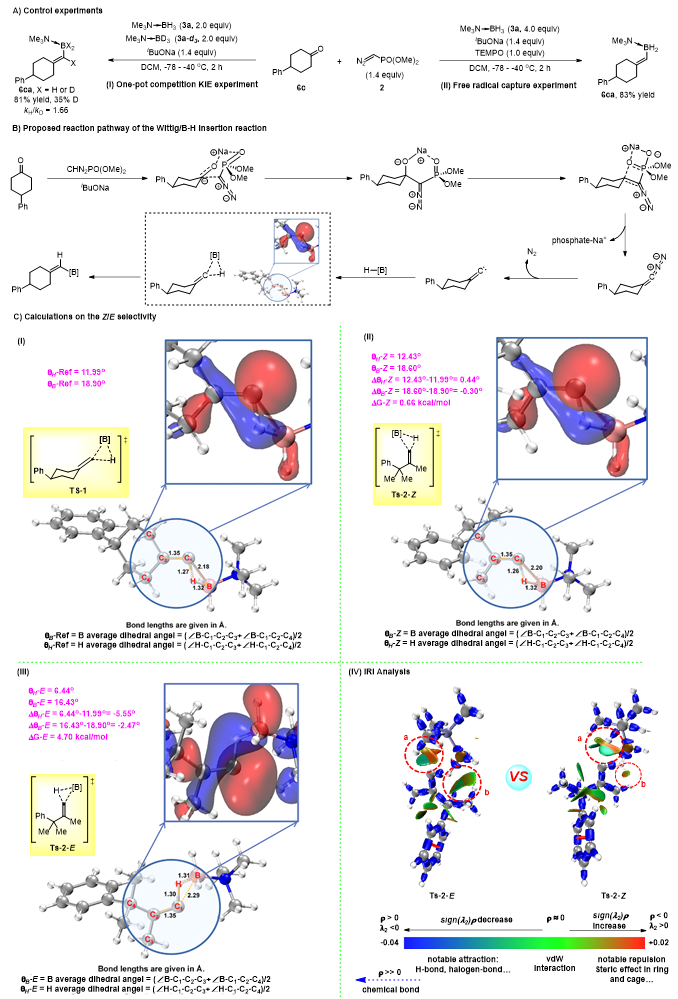
图6. 机理研究
总之,朱守非课题组报道了一类新颖的Wittig/B-H插入反应,可以在脂肪酮化合物中添加一个碳原子并引入一个硼基团来构建烯基硼化合物,给出Wittig反应难以获得的Z-式选择性。这些硼烯烃产物可以进行立体专一的转化得到多种三取代Z式烯烃,具有广阔的应用前景。此外,他们还实现了分子内Wittig/B-H插入反应,从而构建了多种新型非芳香性含硼杂环化合物。DFT计算显示,独特的Z式选择性源于B-H键插入这一基元过程中过渡态轨道最大重叠的需求。该工作拓展了B-H插入的反应类型,深化了对B-H插入反应机理的理解,为三取代Z式烯烃的合成提供了新的实用方法。
