Research: Palladacycle Catalyst Based on a Cyclopropane Monophosphine Ligand for the Suzuki−Miyaura Cross-Coupling Reaction
研究进展:基于环丙烷单膦配体的环钯配合物用于Suzuki−Miyaura交叉偶联反应
Suzuki−Miyaura交叉偶联反应是构建碳-碳键的核心方法,广泛应用于材料科学、药物制造等领域,使其成为众多功能分子合成中不可或缺的化学工具反应(图1a)。含有机配体的钯配合物是该反应最常用的催化剂,其中膦配体因与金属结合能力强、易于制备,且空间位阻和电子性质可灵活调控,应用尤为广泛。然而,目前已有的催化体系仍面临诸多挑战:通常难以兼容含高活性官能团(如端炔、端烯)的底物,该类底物易发生Heck偶联、Sonogashira偶联等副反应导致化学选择性偏低;催化剂负载量普遍较高(>1 mol%)或反应时间过长(>24 h),大幅增加了工业应用成本(图1b)。因此,开发兼具高化学选择性、低负载量、快反应动力学特性的新型钯催化体系,对拓展该反应的应用边界具有重要意义。
南开大学朱守非教授课题组在前期研究中,提出了“基于基元反应的催化剂定向设计(CODER)”策略,成功合成新型环丙烷单膦配体TPhos(Angew. Chem., Int. Ed. 2023, 62, e202309111.。该配体可通过芳基取代基的旋转,灵活调节所得催化剂的反应空腔,精准适配氧化加成与还原消除步骤的空间需求,此前在二芳基胺的Buchwald−Hartwig胺化反应中已展现出优异的反应活性(转化数TON高达340,000,化学选择性高达99%)。在此研究基础上,该课题组进一步制备了TPhos的新型环钯配合物,并系统探究其在Suzuki−Miyaura交叉偶联反应中的应用,最终在催化剂效率与官能团耐受性方面取得了显著突破,最高转化数为192000(图1c)。机理研究表明环钯物种的还原消除得到零价钯物种是启动该反应的关键因素。该研究成果近期发表于Organometallics (2026, 45, 494-503),王佑钦和党玲为论文共同第一作者,朱守非教授和车稳博士为通讯作者。
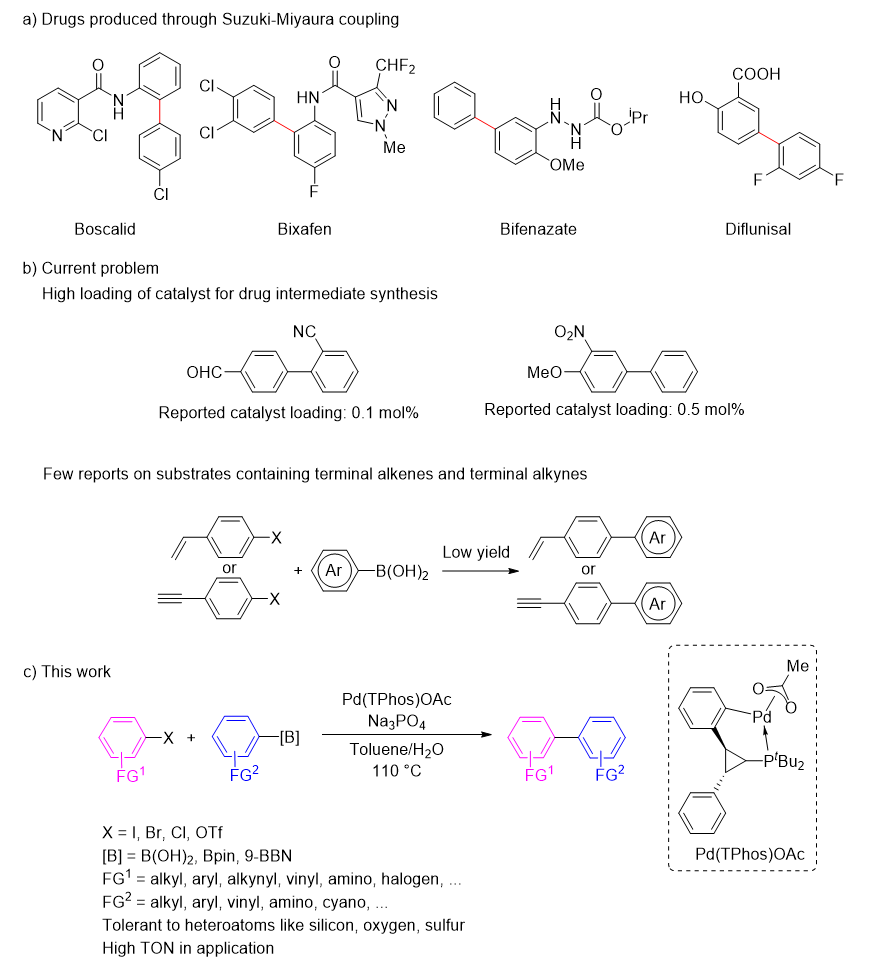
图1 Suzuki-Miyaura偶联反应应用及现存问题
TPhos环钯配合物的合成及结构分析如图2所示:TPhos与乙酸钯配位反应后得到灰白色粉末状环钯配合物,产率达91%。通过对催化剂单晶进行X射线衍射分析发现,该配合物与TPhos配体的苯环形成了钯-碳键,进而构成新型六元环钯配合物。该钯环配合物具有优异的稳定性——在空气中存放2周后,其31P NMR谱图未出现明显变化。
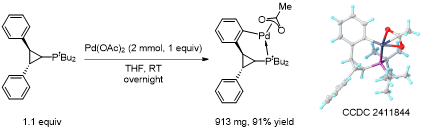
图2 TPhos的环钯配合物的合成及结构分析
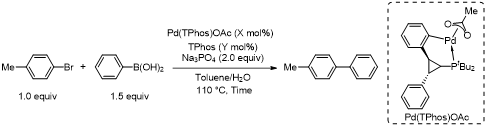
为验证新型环钯配合物的催化性能,研究者以4-溴甲苯和苯硼酸为标准底物,通过筛选碱、溶剂及反应温度,确定了最优反应条件。随后进行高转化数实验(表1),结果显示:当催化剂负载量为0.01 mol%时,反应仅需2 h即可完全转化,产率达97%,转化数(TON)为9700;当催化剂负载量降至0.0005 mol%时,反应仍可顺利进行(反应时间延长至16 h),转化率达99%,产率96%,转化数最高可达192,000;若额外添加0.001 mol%配体,反应时间可缩短至5 h,同时保持192,000的转化数(TON)和96%的产率,转化频率(TOF)达38,400 h-1。
表1 高转化数实验
Entry |
X/mol% |
Y/mol% |
Time/h |
Conv./%b |
Yield/%c |
TON |
1 |
0.01 |
0 |
2 |
100 |
97 |
9700 |
2 |
0.05 |
0 |
11 |
100 |
98 |
19600 |
3 |
0.001 |
0 |
12 |
100 |
97 |
97000 |
4 |
0.0005 |
0 |
16 |
99 |
96 |
192000 |
5 |
0.0005 |
0.001 |
5 |
100 |
96 |
192000 |
研究团队进一步系统探究了该催化体系的底物适用范围,涵盖卤代芳烃底物(图3)、芳基硼酸底物(图4)及烯基、烷基底物(图5)。在卤代芳烃底物范围中,该催化剂表现出优异的官能团耐受性:含对位取代基(烷基、苯基、烯基、炔基、卤素、酯基、羧基、甲酰基、酮羰基、羟基、磺酰基、甲氧基、硝基、氨基、二甲胺基等)的芳基溴化物,均能获得高产率。值得关注的是,对于含乙烯基的溴代芳烃,文献报道的最高转化数仅为1960,而该催化剂可实现4650的转化数;对于含乙炔基的溴代芳烃,文献转化数仅为30,本体系则高达8800。此外,间位取代、邻位取代(包括位阻较大的2,6-二甲基溴苯)的芳基溴,以及萘基、苯并稠杂环、杂芳环类底物,在低催化剂负载量(0.001−0.01 mol%)下均能实现高效转化。对其他离去基团(碘、氯、三氟甲磺酰基)的初步探索表明,此类底物均可获得高产率,但氯代和三氟甲磺酰基取代底物的反应效率相对较低。同时,该体系成功合成了两种常见的炔基取代联苯(A-5、A-22),无需对炔基进行硅基保护,有效克服了现有方法需高催化剂负载量(2−5 mol%)的局限。

图3 卤代芳烃底物类型评价
针对芳基硼酸底物(图4),研究团队以4-溴甲苯为亲电试剂开展实验,结果表明:含对位取代基(烷基、苯基、乙烯基、羟基、氰基、甲酰基、酮羰基、酯基、氨基、甲氧基、三甲基硅基等)的芳基硼酸,均表现出高效反应活性;邻位取代芳基硼酸也能实现高效反应;3,5-二取代芳基硼酸在0.01 mol%催化剂负载量下即可高效转化,但2,6-二取代芳基硼酸(B-18)因易发生脱硼副反应,在0.2 mol%负载量下产率仅为44%(该问题可通过降低反应温度、增加催化剂负载量得以改善)。稠环芳基硼酸(萘基、芘基)同样具有良好的耐受性,产率表现优异。在聚合物合成关键功能单体——乙烯基联苯衍生物的合成中(即4-溴苯乙烯与芳基硼酸的偶联反应),该体系仅需0.05 mol%催化剂,即可在2 h内实现高效转化,其中萘硼酸(B-25)和芘硼酸(B-27)的转化数远超文献报道,有效解决了现有方法“高负载短时间”或“低负载长时间”的痛点。
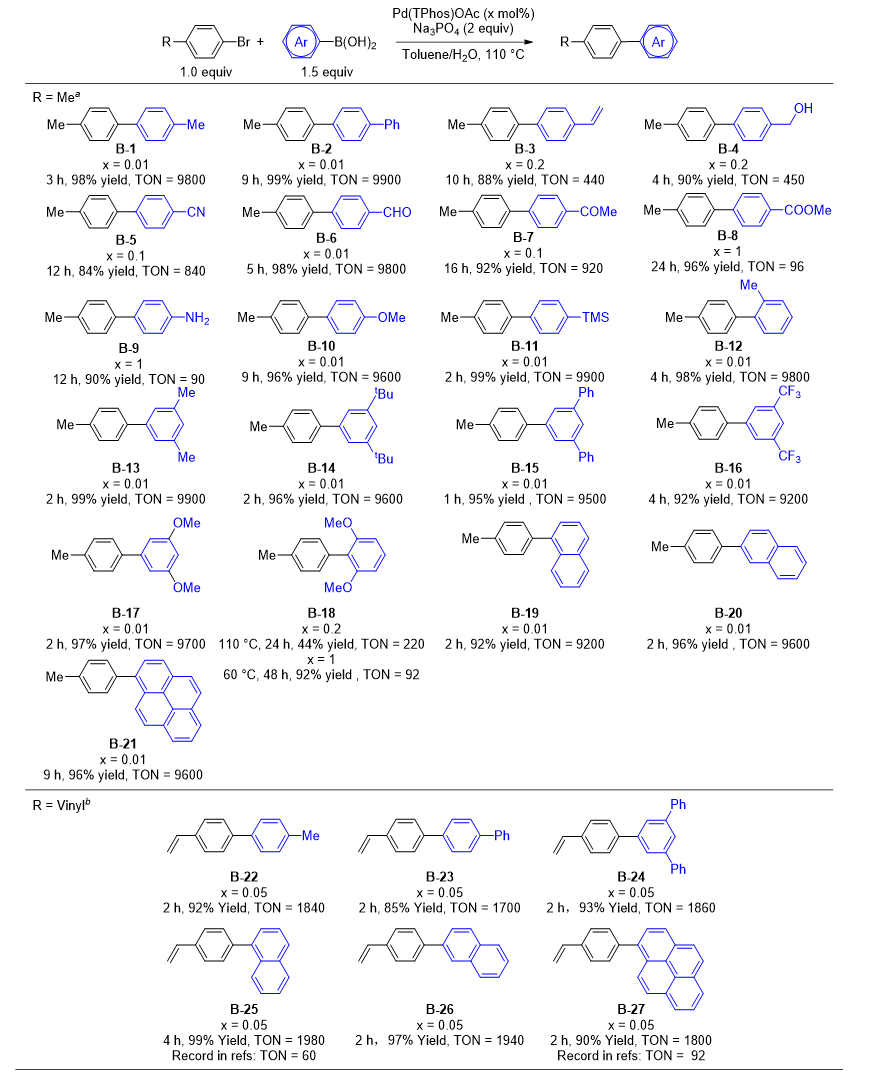
图4 芳基硼酸底物类型评价
该催化体系还成功应用于sp2-sp2偶联(烯基底物)和sp3-sp2偶联(烷基底物)反应(图5)。在烯基底物测试中,烯基亲电试剂(1-溴-2-甲基-1-丙烯,C-1)和烯基亲核试剂(2-甲基-1-丙烯基硼酸频哪醇酯,C-2)均能获得良好产率,其中烯基亲核试剂因反应活性相对较差,需适当提高催化剂负载量。在烷基底物测试中,烷基亲电试剂(1-溴甲基萘,C-3)和烷基亲核试剂(正丁基硼酸,C-4;B-苄基-9-硼杂双环[3.3.1]壬烷,C-5)的产率均超过90%,表现出优异的适用性。
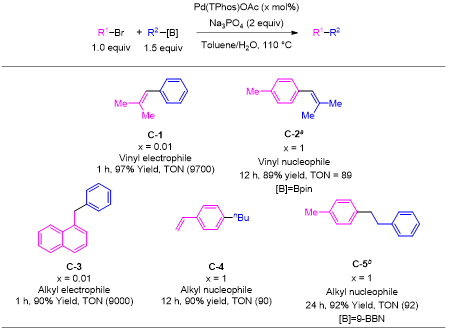
图5 烯基以及烷基底物类型评价
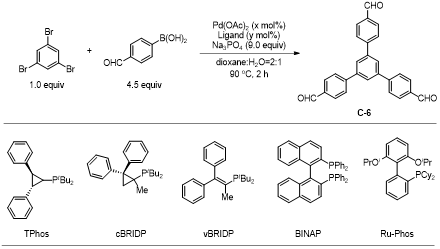
为彰显TPhos配体的优势,研究团队将其与多种商用配体,在共价有机框架(COF)构建单元(对甲酰基苯基)苯的合成中进行对比实验(表2)。结果显示,TPhos的性能显著优于其他商用配体(cBRIDP、vBRIDP、Ad2PnBu、tBu2PnBu、PPh3、Ph2PCy、PCy3、P(4-CF3Ph)3、PtBu3、BINAP、Ru-Phos):在0.1 mol%催化剂负载量下,TPhos可实现底物完全转化,产率高达95%,而多数商用配体需将负载量提升至1 mol%,才能达到相近或更低的产率(其中BINAP在1 mol%负载量下,产率仅为2%)。
表2 COF砌块合成及配体比较
Entry |
Ligand |
x |
y |
Conv./% |
Yield/% |
1 |
TPhos |
0.1 |
0.11 |
>99 |
95 |
2 |
cBRIDP |
0.1 |
0.11 |
>99 |
58 |
3 |
vBRIDP |
0.1 |
0.11 |
>99 |
40 |
4 |
Ad2PnBu |
0.1 |
0.11 |
75 |
65 |
5 |
tBu2PnBu |
0.1 |
0.11 |
>99 |
80 |
6 |
PPh3 |
1 |
1.1 |
>99 |
50 |
7 |
Ph2PCy |
1 |
1.1 |
>99 |
88 |
8 |
PCy3 |
1 |
1.1 |
94 |
65 |
9 |
P(4-CF3Ph)3 |
1 |
1.1 |
>99 |
89 |
10 |
PtBu3 |
1 |
1.1 |
>99 |
72 |
11 |
BINAP |
1 |
1.1 |
45 |
2 |
12 |
Ru-Phos |
1 |
1.1 |
95 |
89 |
为验证该催化体系的实际应用价值,研究团队将其应用于多种药物、农药中间体的克级规模合成(图6)。在沙坦类药物(用于治疗高血压、心绞痛、心力衰竭等)合成中,关键中间体2'-氰基-4-甲酰基联苯(C-7)的现有合成方法需0.1 mol%催化剂负载量,而本体系仅用0.01 mol%催化剂,在90 ℃下反应12 h,即可实现克级规模98%的分离产率。在杀螨剂联苯肼酯(对欧洲叶螨、二斑叶螨等防效显著)的中间体3-硝基-4-甲氧基联苯(C-8)合成中,该体系以极低的0.001 mol%催化剂负载量,实现克级规模90%的分离产率。在丹曲林(用于治疗恶性高热及潜在神经退行性疾病)的中间体5-(4-硝基苯基)-2-呋喃甲醛(C-9)合成中,该体系采用两种市售起始原料,仅需0.1 mol%催化剂负载量,即可实现克级规模84%的分离产率,负载量显著低于现有报道。
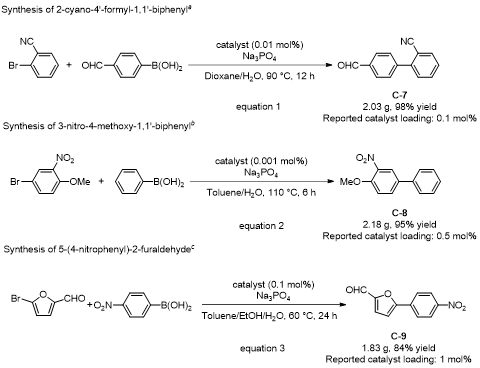
图6 应用与克级规模实验
研究团队还初步探究了TPhos环钯配合物的催化机理(图7)。结合配体对比实验结果,确定TPhos骨架中嵌入的芳基,是实现高催化效率的关键因素。基于此,团队提出反应机理假设:反应通过芳基部分(从苯硼酸转金属化至钯中心)与钯环的芳基发生还原消除而启动,进而生成零价钯(Pd(0))物种。实验验证结果表明:在标准反应条件下,将等摩尔量的环钯催化剂与苯硼酸搅拌36 h后,经硼烷保护处理,成功分离得到还原消除衍生的配体L-1,产率为12%;脱除硼烷保护基后,L-1在0.01 mol%负载量下,表现出与TPhos相当的催化性能,这一结果证实,通过还原消除生成零价钯(Pd(0)),是催化循环的关键启动步骤。
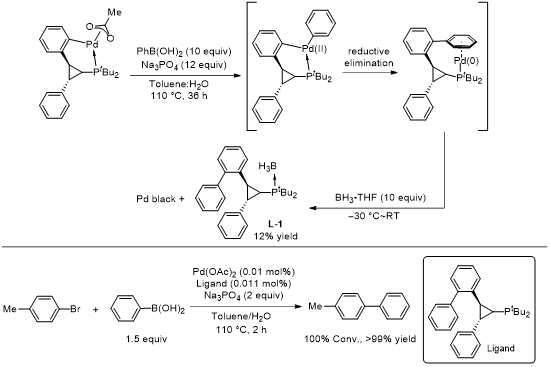
图7 偶联启动机理实验证据
综上,本研究基于环丙烷单膦配体TPhos,成功合成新型六元环钯配合物,并系统探究其在Suzuki−Miyaura交叉偶联反应中的催化性能,发现其兼具高催化效率(最高转化数达192,000)与优异的官能团耐受性,尤其在含端炔、端烯等挑战性官能团的底物反应中,相比现有报道展现出明显优势。其在药物、农药中间体及COF构建单元克级合成中的成功应用,进一步证实了该催化体系的实用价值。
